อะตอม ถูกดึงดูดอยู่กับนิวเคลียสด้วยแรงแม่เหล็กไฟฟ้า
อะตอม ล้อมรอบด้วยกลุ่มหมอกของอิเล็กตรอนที่มีประจุลบ นิวเคลียสของอะตอมประกอบด้วยโปรตอนที่มีประจุบวกกับนิวตรอนซึ่งเป็นกลางทางไฟฟ้า
อะตอม กลุ่มของอะตอมสามารถดึงดูดกันและกันก่อตัวเป็นโมเลกุลได้ อะตอมที่มีจำนวนโปรตอนและอิเล็กตรอนเท่ากันจะมีสภาพเป็นกลางทางไฟฟ้า มิฉะนั้นแล้วมันอาจมีประจุเป็นบวก (เพราะขาดอิเล็กตรอน) หรือลบ (เพราะมีอิเล็กตรอนเกิน)
ซึ่งเรียกว่า ไอออน เราจัดประเภทของอะตอมด้วยจำนวนโปรตอนและนิวตรอนที่อยู่ในนิวเคลียส จำนวนโปรตอนเป็นตัวบ่งบอกชนิดของธาตุเคมี และจำนวนนิวตรอนบ่งบอกชนิดไอโซโทปของธาตุนั้น
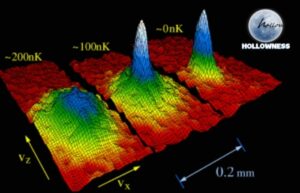
ตามความเข้าใจในปัจจุบัน อะตอมเป็นวัตถุขนาดเล็กที่มีมวลน้อยมาก เราสามารถสังเกตการณ์อะตอมเดี่ยว ๆ ได้โดยอาศัยเครื่องมือพิเศษ เช่น กล้องจุลทรรศน์แบบส่องกราดในอุโมงค์ มวลประมาณ 99.9% ของอะตอมกระจุกรวมกันอยู่ในนิวเคลียส
โดยมีโปรตอนและนิวตรอนเป็นมวลที่เหลือประมาณเท่า ๆ กัน อิเล็กตรอนที่โคจรรอบอะตอมจะมีระดับพลังงานที่เสถียรอยู่จำนวนหนึ่งในลักษณะของวงโคจรอะตอม และสามารถเปลี่ยนแปลงระดับไปมาระหว่างกันได้โดยการดูดซับหรือปลดปล่อยโฟตอนที่สอดคล้องกับระดับพลังงานที่ต่างกัน อิเล็กตรอนเหล่านี้เป็นตัวกำหนดคุณสมบัติทางเคมีของธาตุ
และมีอิทธิพลอย่างมากต่อคุณสมบัติทางแม่เหล็กของอะตอม อิเล็กตรอนของอะตอมถูกดึงดูดกับโปรตอนในนิวเคลียสด้วยแรงแม่เหล็กไฟฟ้า โปรตอนและนิวตรอนในนิวเคลียสถูกดูดเข้าหากันด้วยแรงนิวเคลียร์ ปกติแรงนิวเคลียร์เข้มกว่าแรงแม่เหล็กไฟฟ้า ยกเว้นในบางกรณีที่แรงแม่เหล็กไฟฟ้าเข้มกว่าแรงนิวเคลียร์ ซึ่งจะทำให้เกิดการแบ่งนิวเคลียสและเกิดเป็นธาตุใหม่ เรียกว่า การสลายของนิวเคลียส